- 04/02/2021
- por Resenha Politika
Pandemia
Ministério da Saúde negocia entrega de 30 milhões de doses até março
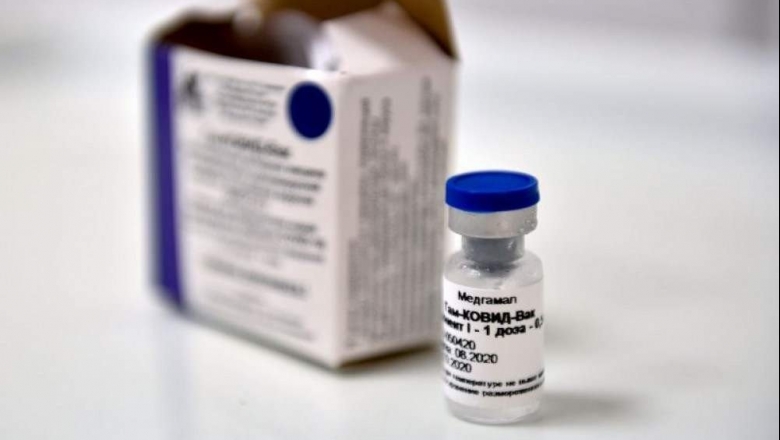
Diante da dificuldade em ampliar a oferta de vacinas contra a covid-19 no Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) dispensou a necessidade de ensaios clínicos de fase 3 no Brasil para autorizar o uso emergencial de vacinas no país, desde que os estudos tenham sido realizados em outros países. A retirada do pré-requisito pode beneficiar a vacina russa SputnikV, produzida no Brasil pela União Química.
A empresa protocolou um pedido para uso emergencial da vacina em 16 de janeiro, mas teve os documentos negados por não atender a todas as exigências regulatórias. Após o anúncio da Anvisa, o Ministério da Saúde informou que negocia a aquisição de 30 milhões de doses prontas, sendo 10 milhões da iniciativa russa e 20 milhões da indiana Covaxin, para entrega até março.
O avanço nas tratativas foi possível por permitir que empresas que têm imunizantes com testes de fase 3 em outro país também possam solicitar esse uso. Neste caso, a Anvisa dispõe de até 30 dias para dar uma resposta, prazo 20 dias maior do que o fornecido para a análise de iniciativas testadas em território nacional.
Por mais que a mudança gere uma expectativa maior em relação à Sputnik V, devido aos recentes anúncios de 91,6% de eficácia, a Anvisa garante que a decisão não foi baseada em nenhum pleito de empresas, do governo ou do Ministério da Saúde. “A atualização desse guia vem junto de estratégias que viemos discutindo para facilitar o acesso [à vacinas] no Brasil”, afirmou a diretora da Anvisa, Meiruze Freitas. A farmacêutica citou o portfólio de vacinas ofertadas pelo mecanismo Covax Facility, que envolve imunizantes sem estudo clínico no Brasil, como ponto que influenciou na decisão.